De detectie van glucose met behulp van een testtrip is gebaseerd op een reactie waarbij het enzym glucose-oxidase een rol speelt. Glucose reageert met zuurstof tot D-glucono-1,5-lactone en waterstofperoxide. In een volgreactie reageert het ontstane waterstofperoxide vervolgens met een zogenoemd chromogeen. Als chromogeen wordt in de teststrip TMB (= 3,3′,5,5′-Tetramethylbenzidine) gebruikt.
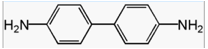 Hiernaast is de structuurformule van benzidine (4,4'-diaminobifenyl) gegeven.
Hiernaast is de structuurformule van benzidine (4,4'-diaminobifenyl) gegeven.
Geef een verklaring voor deze naam.
- Teken de structuurformule van 3,3′,5,5′-Tetramethylbenzidine en leg uit waarom je juist de structuurformule op deze manier hebt getekend.
- Bij de reactie worden de aminogroepen omgezet in imine-groepen; er ontstaat 3,3',5,5'-tetramethylbenzidine diimine. Hierbij is het stikstofatoom met een dubbele binding aan het koolstofatoom uit de ringstructuur verbonden. De reactie is een redoxreactie.
- Geef de halfreactie waarbij waterstofperoxide in zuur milieu als oxidator reageert.
- Geef de halfreactie voor de omzetting van TMB naar het diimine
Ook bij gebruik van het Fehlingsreages is er sprake van een redoxreactie. Fehlings A is een 5% koper(II)sulfaatoplossing. Fehlings B is een oplossing van natriumhydroxide en natriumkaliumtartraat. Een tartraat is een zout dat is ontstaan uit wijnsteenzuur.
- Teken de structuurformule van het tartraat (gebruik binas tabel 66A).
Het tartraation vormt samen met het koper(II)ion een diepblauw gekleurd complex ion.
- Geef een reden voor de aanwezigheid van het tartraation.
De halfreactie voor het Cu2+ ion is als volgt:
2 Cu2+ (aq) + H2O (l) + 2 e- " Cu2O (s) + 2 H+ (aq)
Van glucose is, naast de meest getekende, ringstructuur ook een open-keten-structuur.
- Zoek in binas tabel 66A de naam van de open-keten-structuur en teken de structuurformule.
In de aantoningsreactie reageert glucose tot een zuur volgens de halfvergelijking:
C6H12O6 (aq) + H2O (l) " C6H12O7 (aq) + 2 H+ (aq) + 2 e-
- Geef de totaalvergelijking voor de reactie die optreedt bij gebruik van het Fehlingsreagens waarbij je er rekening mee houdt dat de reactie in basisch milieu plaatsvindt.
- Op welke manier kun je een indruk krijgen van de hoeveelheid glucose die aanwezig is in het monster.
- Leg uit of het Fehlingsreagens kan worden toegepast bij een bloedmonster.

 s
s